Ricerca del professor Wen, Dipartimento di Fisica, The Hong Kong University of
Science and Technology- Hong Kong

L’utilizzo di un microriscaldatore con un sottile strato a base di silicio in un sistema RT-PCR, insieme ad chip microfluidici di vetro-silicio, ha permesso di ridurre il tempo di rilevamento dell’acido nucleico di SARS-CoV-2 a meno di 40 min. Il sistema può raggiungere una velocità di innalzamento della temperatura fino a 30 ° C / s, ed è in grado di completare la rilevazione con una sensibilità fino a 500 copie / ml.

Qi Song,†ab Xindi Sun,†c Ziyi Dai,d Yibo Gao,e Xiuqing Gong,c Bingpu Zhou, d Jinbo Wuc and Weijia Wen
Il virus SARS-CoV-2, provoca una malattia respiratoria acuta, chiamata Covid-19, che ha un’elevata trasmissibilità. Le persone infettate da SARS-CoV-2 possono sviluppare sintomi quali tosse, febbre, polmonite e altre complicazioni, che nei casi più gravi provocano la morte. Una percentuale di persone infette da SARS CoV-2 può essere asintomatica. Al momento, il metodo diagnostico principale per COVID-19 è la
reazione a catena della polimera inversa (RT-PCR), che analizza campioni raccolti tampone rinofaringeo, espettorato e altre secrezioni del tratto respiratorio inferiore. Sono anche in uso altri metodi di rilevamento, ad esempio l’amplificazione isotermica degli acidi nucleici, CRISPR, l’immunocromatografia, il saggio di immunoassorbimento enzimatico (ELISA) e sensori elettrochimici. Poiché gli attuali metodi di analisi vengono eseguiti principalmente presso ospedali centrali e centri di analisi di terze parti, i sistemi di analisi utilizzati impiegano principalmente apparecchiature automatizzate di grandi dimensioni e ad alto rendimento. Data l’attuale situazione dell’epidemia, il test point-of-care (POCT) è vantaggioso in termini di facilità d’uso, maggiore accessibilità da parte dell’utente, rilevamento più tempestivo, accuratezza e sensibilità comparabili, che permettono di ridurre il carico di test sugli ospedali centrali. Il POCT è quindi opportuno per il controllo quotidiano dell’epidemia e il raggiungimento della diagnosi e del trattamento precoci. Questo documento riassume gli ultimi progressi della ricerca nei metodi di rilevamento SARS-CoV-2 basati su POCT, confronta tre categorie di prodotti disponibili in commercio, ovvero test degli acidi nucleici, test immunologici e nuovi sensori, e propone le aspettative per lo sviluppo del rilevamento SARS-CoV-2 basato su POCT, incluso un maggiore accessibilità, maggiore sensibilità e costi inferiori.
Introduzione
Alla fine di dicembre 2019, diversi pazienti con sintomi influenzali sono stati ricoverati negli ospedali di Wuhan, in Cina. Per identificare l’agente patogeno infettivo, i campioni dei pazienti erano sottoposti a sequenziamento dell’RNA metagenomico. I risultati hanno dimostrato che l’agente patogeno era un nuovo coronavirus. Il 30 gennaio 2020, l’Organizzazione mondiale della sanità (OMS) ha definito la polmonite causata dal coronavirus appena scoperto come “malattia respiratoria acuta 2019-nCoV”.
Il 31 gennaio 2020, l’OMS ha proclamato un’emergenza sanitaria pubblica di interesse internazionale (PHEIC). L’11 febbraio 2020, lo studio Coronaviridae Group (CSG) dell’International Committee of Taxonomy ha chiamato questo virus “sindrome respiratoria acuta grave Coronavirus 2 (SARS-CoV-2) ”a causa della sua somiglianza genetica alla sindrome respiratoria acuta grave coronavirus (SARS CoV); i 2 virus appartengono allo stesso ceppo. Successivamente, l’epidemia si è intensificata in una pandemia globale di COVID-19. Le manifestazioni cliniche di COVID-19 variano da sintomi lievi, come tosse, febbre e dispnea, a sindromi pericolose per la vita, come la polmonite e la sindrome da distress respiratorio acuto, e persino morte.
Al momento della stesura di questo articolo, c’erano più di 100 milioni di casi confermati e 2 182 179 decessi. L’alto tasso di infezione e tasso di mortalità per COVID-19 ha causato perdite sostanziali in termini di vita, qualità della vita e economia globale. I ricercatori cinesi hanno imputato l’origine della SARS-CoV-2 ai pipistrelli, ma l’ospite intermedio non è stato ancora determinato. Il genoma di SARS-CoV-2 condivide circa l’89% di omologia di sequenza con pipistrello SARS-like- COVZXC21 e circa l’82% di omologia di sequenza con SARS-CoV umana.
SARS-CoV-2 entra in cellule specifiche attraverso le interazioni proteina-proteina: la glicoproteina S di SARS-CoV-2 si lega all’enzima di conversione dell’angiotensina 2 (ACE2) sulle superfici di alcuni tipi di cellule. Attraverso il processamento da parte della proteasi TMPRSS2, il virus, attaccato sulla superficie cellulare, entra nelle cellule. La proteina S è composta da 2 subunità funzionali: S1 e S2. La subunità S1 si lega a recettori delle cellule ospiti, mentre la subunità S2 fonde la membrana virale e la membrana cellulare.
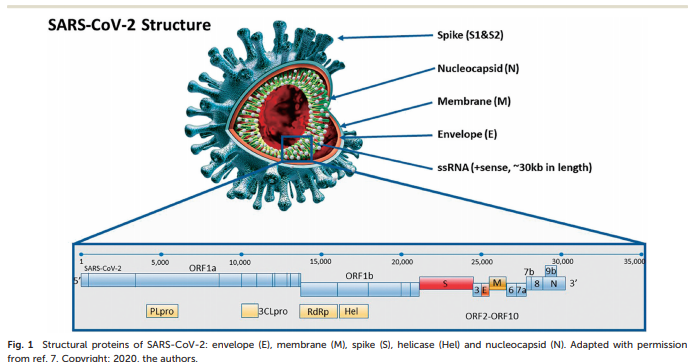
Le proteine strutturali della SARS CoV-2, cioè l’involucro (E), la membrana (M), l’elicasi (Hel) e le proteine del nucleocapside (N), sono mostrate in Fig. 1.7 La replicazione virale richiede altri geni ausiliari, tra cui open read ing frame 1a (ORF1a), ORF1b, RNA-dipendente RNA polymer ase (RdRp) ed emoagglutinina esterasi ( HE). La proteina M è la proteina più abbondante sulle particelle virali. La proteina E è la più piccola proteina strutturale principale di SARS-CoV-2 ed è coinvolta nell’assemblaggio, rilascio e patogenesi del virus.
La proteina N è la principale proteina strutturale della SARS CoV-2. È responsabile della trascrizione e della replica dell’RNA virale, il confezionamento del genoma avvolto in particelle virali e le interazioni con il ciclo cellulare delle cellule ospiti.
La proteina N è la proteina fosforilata più abbondante prodotta e rilasciata durante l’infezione virale. Ha un’elevata immunogenicità e può essere rilevato nel siero o nelle urine all’interno le prime due settimane di infezione. Rilascio della proteina N da parte del virus raggiunge il picco circa dieci giorni dopo l’infezione.
Le principali vie di trasmissione di SARS-CoV-2 sono il contatto e la trasmissione di goccioline. Ad esempio, goccioline da un individuo infetto si depositano sulle superfici di oggetti; se un individuo non infetto tocca la superficie di un oggetto contaminato e quindi tocca le sue membrane mucose del cavo orale, della cavità nasale e degli occhi, si puo’ verificare l’infezione può . Inoltre, inalazione diretta delle goccioline generate da individui infetti quando tossiscono / starnutiscono / parlano o
anche la respirazione da parte di individui a distanza ravvicinata possono provocare infezioni. Pertanto, la diagnosi precoce dei casi sospetti è un compito importante nella gestione degli individui infetti e nel controllo della diffusione di agenti patogeni.8 L’OMS sottolinea che l’identificazione precoce e l’isolamento sono essenziali per limitare trasmissione da uomo a uomo.
Pertanto, è necessario condurre uno screening efficace su larga scala utilizzando sensibilità e metodi di rilevamento ad alto rendimento; questo approccio di screening
consente l’identificazione, l’isolamento e il tracciamento delle persone senza sintomi evidenti, facilita una riduzione delle infezioni secondarie tra contatti stretti e operatori sanitari e porta a miglioramenti nel controllo locale. Inoltre, lo screening fornisce informazioni per il controllo delle malattie a livello regionale e previene l’ulteriore diffusione di infezioni.
Allo stato attuale, i metodi per la rilevazione di COVID-19 includono principalmente test degli acidi nucleici e test sierologici.
Questi metodi sono adatti per la diagnosi in vitro dei pazienti con sospetta infezione da SARS-CoV-2. Il test degli acidi nucleici comprende il sequenziamento genico, la reazione a catena della polimera inversa (RT-PCR) e altri metodi. Nella fase iniziale di nuovo focolaio di coronavirus, la sequenza del genoma del virus SARS-CoV 2 è stata ottenuta tramite sequenziamento genico, fornendo una base importante per i test successivi.
RT-PCR è considerata gold standard per la rilevazione di COVID-19, soprattutto all’inizio dello stadio dell’infezione virale. Mirando all’esclusiva sequenza di RNA di SARS-CoV-2, il materiale genetico dell’agente patogeno può essere rilevato direttamente mediante RT-PCR.
Tuttavia, i test quantitativi RT-PCR (RT-qPCR) attualmente disponibili variano considerevolmente in sensibilità, stabilità e tempo di rilevamento. Inoltre i costi del test sono piuttosto alti. Questi test sono adatti principalmente per grandi laboratori diagnostici centralizzati.
Inoltre, il tempo richiesto per il trasporto del campione supera di gran lunga il tempo impiegato sui test, ritardando ulteriormente la diagnosi.
I test sierologici implicano l’uso di campioni di sangue per rilevare i virus. I due principali anticorpi testati nel sangue sono immunoglobuline G (IgG) e
immunoglobulina M (IgM). Attualmente, il test sierologico per COVID-19 prevede principalmente la misurazione diretta degli antigeni e la rilevazione indiretta di anticorpi nel siero. Anche il test di immunoassorbimento enzimatico (ELISA) è un metodo sensibile per rilevare COVID-19. Anche l’imaging gioca un ruolo importante in
la diagnosi e il trattamento di COVID-19, soprattutto nella fase di inizio della malattia
A causa del rapido sviluppo di COVID-19 e della limitata capacità di rilevamento molecolare basato sul laboratorio, un rapido metodo del test al point-of-care (POCT) è urgentemente necessario per facilitare la diagnosi di COVID-19 al di fuori del contesto di laboratorio.
Metodi POCT, come alcuni test rapidi di diagnosi del contagio forniscono risultati entro pochi minuti dalla somministrazione del test consentendo decisioni rapide sulla cura del paziente. Questi dispositivi sono economici e facili da usare, fornendo tempo sufficiente per l’attuazione delle necessarie misure preventive o terapeutiche. Quindi anche i dispositivi POCT possono estendere i test a comunità e popolazioni che non possono accedere prontamente alle cure. Come citato dalle linee guida del test POC da Centri degli Stati Uniti per il controllo e la prevenzione delle malattie (CDC), i test POC vengono utilizzati per diagnosticare COVID-19 in vari ambienti, come studi medici, strutture di assistenza urgente, farmacie, cliniche sanitarie scolastiche, strutture di assistenza a lungo termine, case di cura, così come alcuni luoghi temporanei, come siti drive-through gestiti da organizzazioni locali.
Nel nostro articolo di revisione, il test POC, in particolare per il test COVID-19,
si riferisce principalmente a uno scenario di test in cui un professionista potrebbe eseguire un test veloce e frequente, come sopra menzionato.
Poiché i paesi affrontano la pandemia COVID-19 in modo variabile, un’area di accordo è la necessità di testare il virus COVID 19 in quante più persone possibile. Come riportato dai media nel Regno Unito, l’accesso al test COVID-19 (virale) è stato limitato per alcune fasce della popolazione, compresi gli operatori sanitari. Ci sono stati anche lunghi ritardi nel riportare i risultati alla persona sottoposta a test che evidenziano la necessità di una maggiore frequenza di test, una maggiore possibilità di trovare una persona contagiosa. Il merito maggiore di POCT è la possibilità di eseguire i test con una elevata frequenza. Potremmo scoprire immediatamente le persone contagiose invece di consegnare il campione a un laboratorio centrale
laboratorio di analisi e attendere molto tempo per un risultato del test.
POCT non significa mancanza di accuratezza. Di solito, una macchina POCT
ha la stessa sensibilità e specificità di quella utilizzata nel laboratorio centrale. Soprattutto, alcuni strumenti POCT sono dotati di moduli di rilevamento automatizzati mediante i quali potrebbero essere realizzate procedure di prova di campionamento e risposta. Ciò non solo riduce la complessità dell’operazione, ma aumenta anche la sensibilità del test attraverso un processo automatico.
Nel presente documento, esaminiamo i metodi POCT esistenti e in fase di sviluppo, per la rilevazione del COVID-19; questi metodi includono test degli acidi nucleici, test immunologici sierologici, piattaforme microfluidiche e strumenti portatili utilizzati per la diagnosi rapida standard di COVID 19. Riassumiamo ed evidenziamo anche vari sistemi di rilevamento rapido tecnologie e strumenti portatili per la rilevazione di
il nuovo coronavirus.
POCT basati su acidi nucleici
Per rilevare l’acido nucleico SARS-CoV-2, il primo passo è raccogliere
fluidi biologici dalle regioni corporee in cui si trova il virus. I fluidi sono di solito raccolti utilizzando tamponi nasofaringei e tamponi orofaringei. I fluidi raccolti vengono sottoposti a una serie di fasi di filtrazione e isolamento per ottenere il virus. La tecnologia microfluidica consente la miniaturizzazione e l’integrazione della purificazione degli acidi nucleici e dell’amplificazione PCR su larga scala e ne migliora l’efficienza.
Dopo l’estrazione dell’RNA, la trascrizione inversa viene utilizzata per generare il DNA complementare (cDNA) di RNA virale. Successivamente, specifiche regioni del cDNA sono amplificate, in presenza di sonde a DNA, mediante PCR, realizzando così la rivelazione in tempo reale del processo di amplificazione.
Al momento, i test degli acidi nucleici per il SARS-CoV-2 comprendono principalmente RT-PCR, amplificazione isotermica mediata da loop (LAMP) e test basati sulle proteine Cas (CRISPR-associated). Questa sezione presenta gli ultimi risultati della ricerca scientifica e gli strumenti POCT in commercio.
Test basati sulla RT-PCR
La PCR è una reazione biochimica controllata dalla temperatura e catalizzata da enzimi. Gli strumenti per la PCR sono termociclatori che controllano principalmente 3 cicli termici: denaturazione a circa 95°, rinaturazione a circa 55° e allungamento a circa 72°. Ogni ciclo PCR porta all’aumento esponenziale del numero dei frammenti di DNA, producendo dunque una grande quantità di una specifica sequenza genica in un determinato periodo di tempo. In un convenzionale termociclatore da banco, le reazioni avvengono in provette eppendorf e gli sbalzi di temperatura di 20° vengono completati in 10 s. Con i chip per DNA, gli stessi sbalzi termici di ottengono in meno di 1 s grazie alla miniaturizzazione, la ridotta capacità termica e la maggior conduttività termica, aumentando così l’efficienza del processo.
Per esempio, Wu et al. hanno creato un dispositivo PCR per una rapida amplificazione ed un rapido rilevamento del DNA. Come mostrato nella figura accanto
Per esempio, Wu et al. hanno creato un dispositivo PCR per una rapida amplificazione ed un rapido rilevamento del DNA. Come mostrato nella figura accanto, questo dispositivo consiste in una camera di reazione PCR intercambiabile, un sistema di controllo della temperatura e un sistema di rilevamento ottico. Il sistema di controllo della temperatura è in grado di controllare la temperatura con un’elevata precisione e con un efficiente tasso riscaldamento/raffreddamento. Il chip per la PCR è indipendente dal sistema di controllo della temperatura e dal sistema di rilevamento ottico.
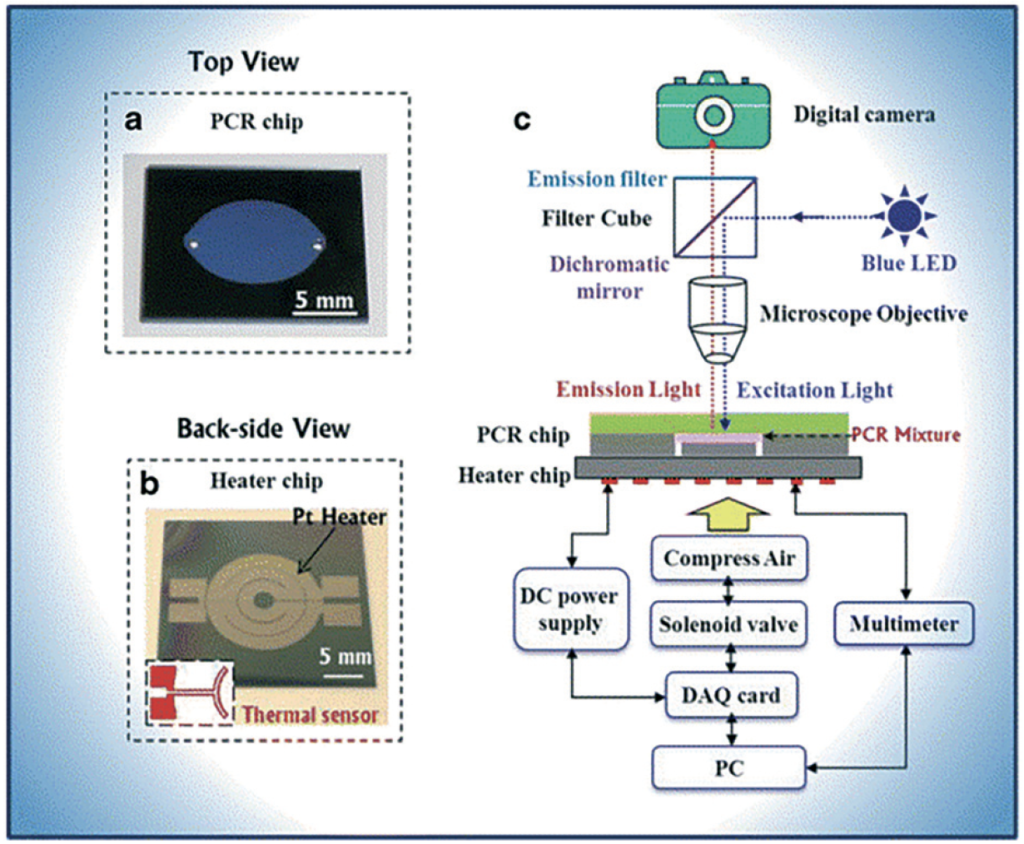
Ci sono altri sistemi microfluidici a riscaldamento rapido basati sul riscaldamento a infrarossi, ad aria ed a microonde. Questi sistemi privi di contatto hanno una maggior velocità di riscaldamento (65 °C/s) e un’elevata precisione della temperatura (+/- 0.1 °C). Considerando che la RT-PCR può potenzialmente rilevare una singola copia di RNA in una reazione, è al momento considerata il gold standard per la diagnosi del Covid-19. Ci sono molte sequenze target sull’RNA del SARS-CoV-2 che possono essere utilizzate per il rilevamento mediante PCR. La metodica standardizzata dall’OMS per l’esecuzione di un test molecolare per Covid-19 comprende le fasi di raccolta del campione, trasporto del campione, analisi del campione e analisi dei risultati. La raccolta del campione consiste principalmente nella raccolta di campioni mediante tamponi rino/orofaringei, di campioni di espettorato o di campioni salivari. I tamponi rino/oro-faringei sono utilizzati per la raccolta di materiale del tratto respiratorio superiore. Tale raccolta deve essere eseguita da staff medico che deve trovarsi a stretto contatto con il paziente, esponendo così l’operatore sanitario ad un certo rischio di infezione.
Considerando che il tasso tamponi orofaringei “falsi negativi” influenza la formulazione della diagnosi, Chen et al. hanno utilizzato dei patch con microaghi per progettare degli swab grazie ai quali è possibile incrementare la qualità e la quantità della raccolta del virus. L’anticorpo per la proteina virale spike è stato incorporato nel patch di microaghi per migliorare l’efficienza di raccolta del campione e ridurre così i “falsi negativi”. L’espettorato, che può essere raccolto in maniera non invasiva, permette la raccolta dal tratto respiratorio inferiore. Lin et al. hanno diagnosticato il Covid-19 attraverso l’analisi RT-PCR di campioni di espettorato. Tuttavia, in uno studio su 41 pazienti, solo il 28% di questi ha fornito un campione di espettorato adatto alla diagnosi. Risultati di RT-PCR del laboratorio di Hong Kong dell’OMS hanno dimostrato che da tamponi faringei è possibile determinare la positività al SARS-CoV-2. Uno studio ha dimostrato che la saliva presenta una quantità di particelle virali paragonabili a campioni rinofaringei con una specificità del 90%. In più, raccogliere la saliva è un processo molto più semplice che può essere effettuato direttamente dal paziente, andando così a ridurre il rischio di infezione per l’operatore sanitario. Utilizzando il gene S come target, Kelvin KW To et al. hanno raccolto campioni salivari da pazienti positivi al Covid-19 e eseguito test 1-step RT-PCR. Il virus è stato rilevato in 11 pazienti su 12.
I primer per la RT-PCR sono stati costruiti per diverse sequenze target del genoma di SARS-CoV-2. Chu et al. hanno sviluppato due metodi di 1-step RT-PCR per il rilevamento delle regioni ORF1b e N del genoma virale. Il gene altamente conservato RdRp e il gene variabile S sono stati introdotti come target in uno studio successivo. Nel test RT-PCR sviluppato dalla compagnia tedesca Tib-Molbiol, il gene E del SARS-CoV-2 è stato usato per i primi screening, mentre il gene RdRp è stato usato per confermare la diagnosi. Questo test è altamente specifico per il SARS-CoV-2 e non ha mostrato alcuna cross-reazione con altri coronavirus. Chan et al. hanno sviluppato tre metodi di rilevamento RT-PCR utilizzando come target le regioni RdRp/Hel, S e N e ne hanno messo a confronto i risultati. Tra questi tre metodi, quello che rilevava la presenza di RdRp/Hel aveva una maggior sensibilità e specificità.
Shen et al. hanno sviluppato un sistema microfluidico integrato contenente un chip microfluidico con un array di emoagglutinina/neuraminidasi. Questo sistema permette la purificazione automatica del virus, lisi virale, 1-step RT-PCR e rilevamento del segnale fluorescente. Microbiglie magnetiche vengono utilizzate per l’estrazione e l’isolamento del virus, mentre microvalvole controllate pneumaticamente sono utilizzate per il controllo dei liquidi sul chip. Con questo sistema microfluidico, possono essere simultaneamente rilevati fino a 12 sottotipi del virus dell’influenza A in meno di 100 minuti, con una velocità di analisi significativamente maggiore rispetto ad altri metodi.
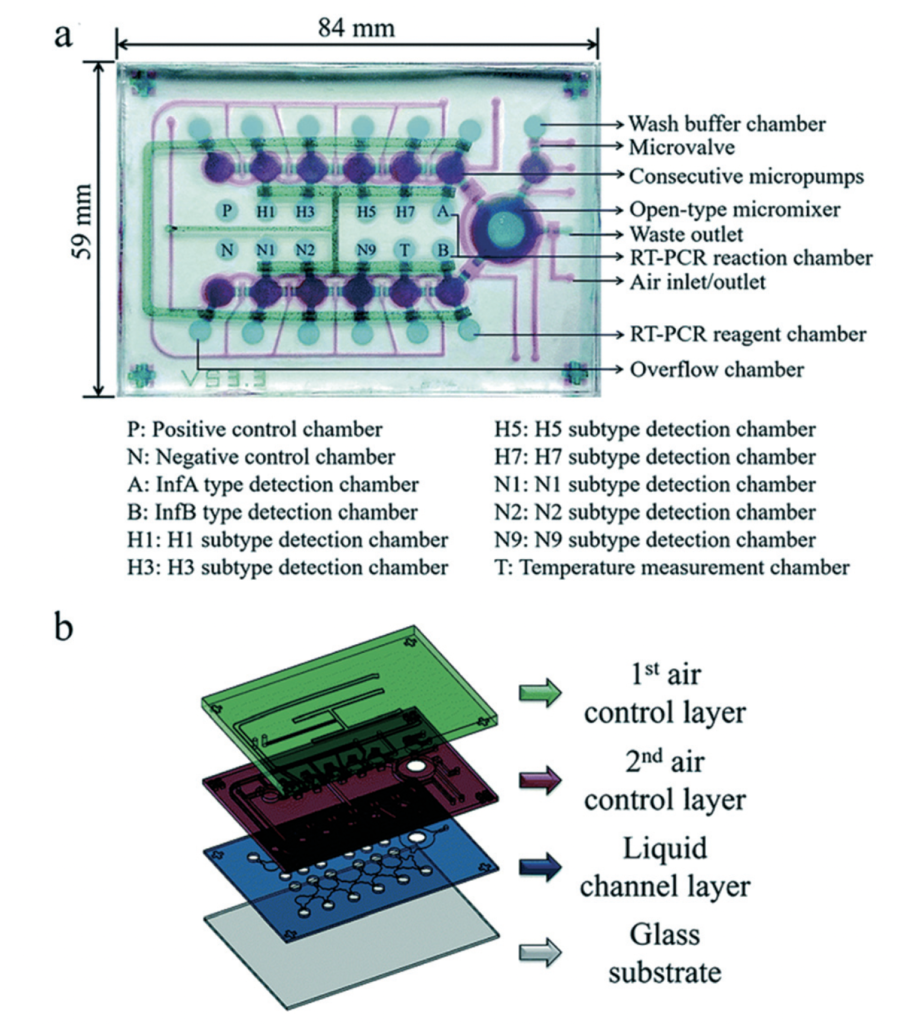
La struttura del chip microfluidico è mostrata nella figura sulla sinistra. Il chip ha una lunghezza di 84 mm, una larghezza di 59 mm e una profondità di 10 mm. E’ costituito da uno spesso strato di polidimetilsilossano (PDMS) per il controllo dell’aria, un sottile strato di PDMS con canali microfluidici e uno strato di vetro per sigillare il chip microfluidico. Il processo per il rilevamento del virus dell’influenza A è il seguente.
Prima di tutto le microbiglie magnetiche, il campione contenente il virus, i reagenti RT-PCR e un buffer per il lavaggio vengono caricati nei canali corrispondenti. Il virus è poi isolato grazie alle microbiglie e il complesso virus-microbiglie è a sua volta isolato grazie all’azione di un campo magnetico esterno generato da un magnete. Successivamente, un raffreddatole termoelettrico è posto sotto il chip. L’RNA virale è rilasciato mediante lisi termica e trasportato alla camera di reazione per la RT-PCR (40 cicli di reazione). infine, i segnali generati dalla RT-PCR vengono rilevati mediante un modulo ottico di rilevamento.
Strumenti POCT basati su acidi nucleici attualmente in commercio
segue…


